認知症とは 〜アルツハイマー型が約半数を占める〜
「認知症」とは、さまざまな脳の病気により、脳の神経細胞の働きが徐々に低下し、認知機能(記憶、判断力など)が低下して、
社会生活に支障をきたした状態のことをいいます。
日常生活上では、ミスが増える、以前のように食事を作れなくなる、お金の管理がうまく出来なくなる、などの変化が現れてきます。また、認知症には、不安、うつ症状、幻覚、妄想、不眠、興奮などの行動・心理症状を伴うこともあり、およそ6ヶ月以上この状態が続く場合に認知症と診断される可能性があります。65歳以上から発症率が上がり、85歳以上では4人に1人が発症します。また団塊の世代が全員75歳以上の後期高齢者になる2025年には約700万人になると言われています。
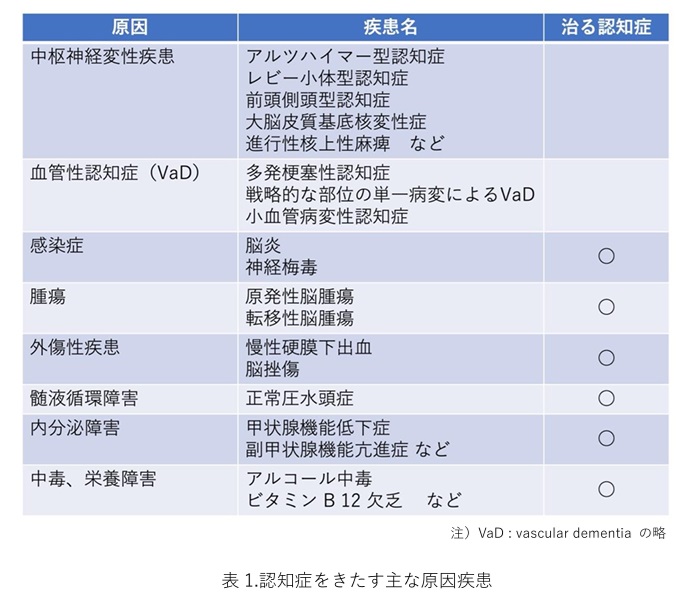
最も多いのはアルツハイマー型認知症(アルツハイマー病)で、約半数を占めています。その他には、脳梗塞に引き続いておこる脳血管性認知症、幻視を伴うレビー小体型認知症(レビー小体病)、前側頭型認知症などがあります。アルコール多飲も認知症の代表的な原疾患です。特に大量飲酒者において、ビタミンB1欠乏が合併することでウェルニッケ・コルサコフ症候群(Wernicke-Korsakoff Syndrome)が発症します。この際には脳内で急速に神経細胞障害が生じており、急性期には痙攣や意識障害から死に至ることがあり、慢性期には認知症をきたします
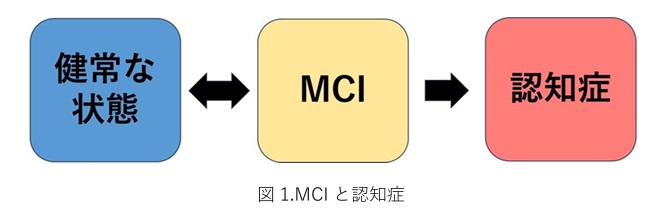
軽度認知障害 〜認知症の手前の状態(グレーゾーン)〜
軽度認知障害(MCI:Mild Cognitive Impairment)とは、認知症になる一歩手前の状態を指します。記憶力の低下がみられますが、基本的な日常生活には支障をきたさない状態で、認知症のグレーゾーンと言えます。軽度認知障害のことを、厚生労働省は、以下のように定義しています。
1)年齢や教育レベルの影響のみでは説明できない記憶障害が存在する
2)本人または家族による物忘れの訴えがある
3)全般的な認知機能は正常範囲である
4)日常生活動作は自立している
5)認知症ではない
すなわち、『記憶力に障害があって物忘れの自覚があるが、記憶力の低下以外に明らかな認知機能の障害がみられず、日常生活への影響はないか、あっても軽度のものである場合のこと』で、認知症の前段階と考えられています。
MCIでは、1年で5~15%が認知症に移行する一方、1年で16~41%は健常な状態に戻ることがわかっています。そのため、早期から認知症予防の対策を行うことが重要で、適切な認知症予防策をすることにより、健常な状態への回復や認知症への移行を遅らせることが出来ます。
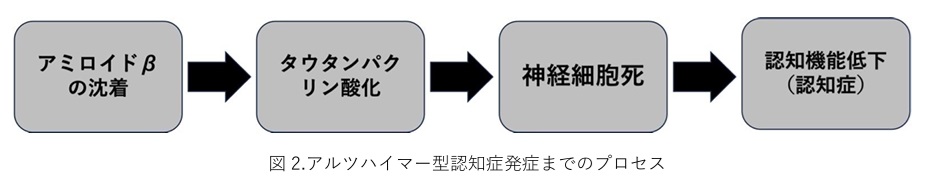
アルツハイマー型認知症の原因 〜アミロイド仮説〜
認知症の約半数を占めるアルツハイマー型認知症の発症は、神経細胞へのアミロイドβ(異常なタンパク質のこと)の沈着が引き金となり、神経細胞内の物質輸送に関わるタウタンパクがリン酸化されることにより物質輸送の機能低下が起こり、その結果、神経細胞機能が低下し、脳が萎縮(神経細胞死)するために起き(アミロイド仮説)と言われています。発症の機序には諸説がありますが、その中で現在最も有力とされているのがこの「アミロイド仮説」です。そして、神経細胞が壊れることで、神経伝達物質アセチルコリンが関わる神経系の障害などが起こり、アセチルコリンの量が減ってしまい、認知機能の低下があらわれます。
糖尿病・糖代謝異常も、アルツハイマー型認知症の危険因子と言われており、糖尿病の人は、アルツハイマー型認知症の罹患率が2倍になると言われています。インスリンはアミロイドβの代謝に様々な影響を与えていると考えられています。インスリンを体内で分解する「インスリン分解酵素」はインスリンの他にアミロイドβも分解します。糖尿病により血中が高インスリン状態になれば、脳内の「インスリン分解酵素」によるアミロイドβの分解量が相対的に低下し、結果的にアミロドβの沈着につながる可能性があります。また「インスリン分解酵素」は、タウタンパクのリン酸化も促進すると言われており、糖尿病はアルツハイマー型認知症の病態に深く関与していると考えられています。
薬物療法 〜4成分の治療薬〜
認知症の症状の進行は、お薬により遅らせることが出来る場合があります。しかし、認知症を完治させることは出来ません。あくまでも進行を遅らせるだけなので、軽症のうちから治療を開始することで症状の軽い状態を保たせることしか出来ません。
1)コリンエステラーゼ阻害薬
原因の項で「神経細胞が壊れることで、神経伝達物質アセチルコリンが減ってしまう」と説明しましたが、減ってしまったアセチルコリンを増やしてくれるのが「コリンエステラーゼ阻害薬」です。アセチルコリンは脳内でコリンエステラーゼという酵素により分解されます。コリンエステラーゼの働きを阻害することができれば、アセチルコリンの働きを増強する効果が期待出来ます。
2)NMDA受容体拮抗薬
脳には神経細胞を興奮させる「グルタミン酸」という神経伝達物質があります。認知症患者ではこのグルタミン酸が過剰になっており、このグルタミン酸によって、脳内で神経に情報を伝えるNMDA(N-methyl-d-aspartate)受容体が過剰に活性化され、神経細胞や記憶に障害が現れます。この過剰なNMDA受容体の働きを抑えるのが「NMDA受容体拮抗薬」です。
日本で使用出来る4成分の既存治療薬の特徴を簡単にまとめてみました。
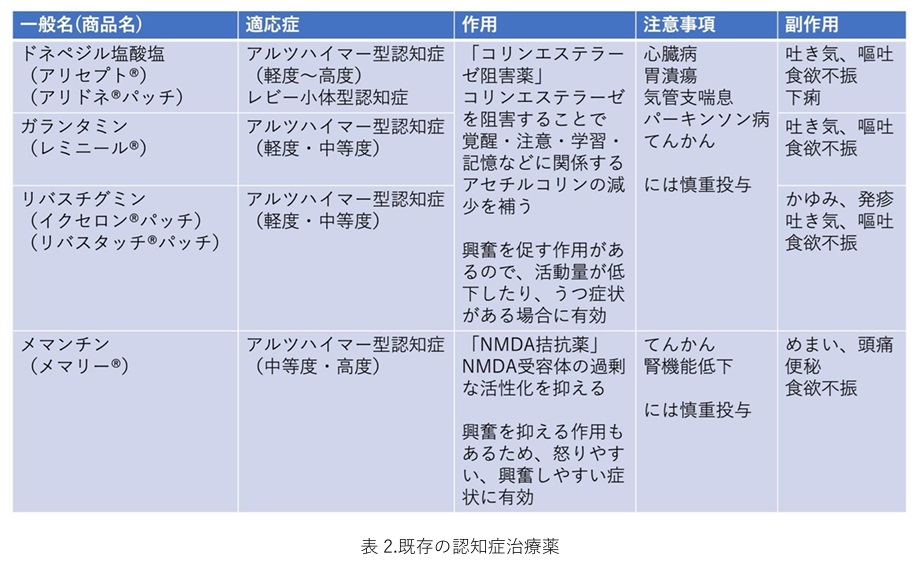
新しい認知症治療薬 〜アミロイド仮説に基づく治療薬〜
新しい治療薬が、2023年9月に日本で承認され、同年12月に発売となりました。アリセプト®の製造販売元の「エーザイ」が米国のバイオ医薬品会社「バイオジェン」と共同開発した「レケンビ®点滴静注」(一般名;レカネマブ)です。欧州(EU)、中国、カナダ、英国(北アイルランドを除く)、韓国においても、それぞれ承認申請を行っており、米国(2023年1月発売)、日本に続き、2024年1月には中国でも承認されました。このお薬は、「ヒト化抗ヒト可溶性アミロイドβ凝集体モノクローナル抗体」と呼ばれており、アルツハイマー型認知症の原因と言われているアミロイドβにくっついて、その量を減らしてくれます。その結果、神経細胞の破壊を抑え、進行を遅らせることが出来ます。大規模グローバル臨床第Ⅲ相試験Clarity AD試験の結果によると、CDR-SB(Clinical Dementia Rating Sum of Boxes;全般臨床症状の評価指標のこと)における18カ月時点の臨床症状の悪化をプラセボと比較して27%抑制しました。また、副次評価項目の一つである、衣服の着脱、食事、地域活動への参加など当事者様が自立して生活する能力を介護者が評価するADCS MCI-ADL(AD Cooperative Study-Activities of Daily Living Scale for Mild Cognitive Impairment)においては、プラセボと比較して37%の有意差が認められました。
投与方法は2週間に1回の点滴静注です。副作用で、脳の浮腫・微小出血(12〜13%)が最初の数ヶ月に多く起こるため、2ヶ月に1回はMRI検査を行わなくてはいけません。
治療の対象となるのは認知症を発症する前の「軽度認知障害」の人や、アルツハイマー型認知症の発症後早い段階の人となっています。どのくらい早期かといと、少し物忘れがある程度で認知症かどうか症状だけでは区別が付かない程度の段階です。また、「軽度認知障害」や「軽度の認知症」である事と同時に、脳中にアミロイドが蓄積していることを証明する必要があります。物忘れがあっても検査でアミロイドがなければこのお薬を使用することは出来ません。アミロイドの脳内沈着を証明するにはPET検査等を行う必要があるのですが、実施出来る施設が限られているので気軽にどこの施設でも行えるものではありません。
治療を行う医師にも条件があり、「日本神経学会」「日本老年医学会」「日本精神神経学会」「日本脳神経外科学会」のいずれかの専門医である必要があります。また、「レケンビ®点滴静注」は生物学的製剤であるため、治療費が高額になることが予想されます。例えば体重50kgの患者さんの場合、1ヶ月のお薬代(診察費等は含めず薬の値段のみ)を計算してみると、1割負担で22,888円、3割負担では68,665円になります。
最後に
1999年に日本で初めての認知症治療薬としてアリセプト®が発売されました。その後2011年にレミニール®・イクセロン®・リバスタッチ®・メマリー®が立て続けに上市されてから10数年間、新薬は出ていませんでした。ようやく2023年4月にアリドネ®パッチが発売されましたが、成分はアリセプト®と同じドネペジルでした。そして、今回ようやく新成分の「レケンビ®点滴静注」が発売されました。しかし、点滴静注であるため頻繁に医療機関に通う必要があること、診断の煩わしさ、治療を行う医師に制限があること、医療費が高額になることなど様々な問題があり、これまでの4成分の治療薬のように一般に広く使われるお薬になるかは疑問です。
参考文献
アリセプト®・アリドネ®パッチ・メマリー®・リバスタッチ®パッチ・レケンビ®点滴静注・レミニール®添付文書
大阪市立大学 医学研究科 認知症病態学 ホームページ
厚生労働省 e-ヘルスネット
厚生労働省 適正使用推進ガイドライン レカネマブ(遺伝子組換え)
Biogenホームページ
国立研究開発法人 国立長寿医療研究センター MCIハンドブック
糖尿病 58(8):535~537,2015
日本老年医学会雑誌 57巻 1 号(2020:1)





